
技術文(wen)章(zhang)
Technical articles 熱門搜索(suo):
摩方精(jing)密3D打印(yin)
2微(wei)米(mi)高精(jing)度微(wei)納(na)3D打印(yin)系(xi)統(tong)
microArch S240A10μm高精(jing)度微(wei)納(na)3D打印(yin)
器官(guan)芯(xin)片3d打印(yin)
nanoArch P14010μm精(jing)度微(wei)納(na)3D打印(yin)系(xi)統(tong)
nanoArch S1302μm精(jing)度微(wei)納(na)3D打印(yin)系(xi)統(tong)
微(wei)納(na)陶瓷(ci)3D打印(yin)服(fu)務
nanoArch S14010μm精(jing)度微(wei)納(na)3D打印(yin)系(xi)統(tong)
nanoArch P15025μm高精(jing)密3D打印(yin)系(xi)統(tong)
3D打印(yin)微(wei)針
microArch S240A光固(gu)化陶(tao)瓷(ci)3D打印(yin)機(ji)
微(wei)流控(kong)芯(xin)片3D打印(yin)
精(jing)密連接(jie)器3D打印(yin)
10微(wei)米(mi)高精(jing)度微(wei)納(na)3D打印(yin)系(xi)統(tong)
nanoArch S1403d打印(yin)精(jing)密醫(yi)療(liao)內(nei)窺鏡
光固(gu)化3D打印(yin)
熱門搜索(suo):
摩方精(jing)密3D打印(yin)
2微(wei)米(mi)高精(jing)度微(wei)納(na)3D打印(yin)系(xi)統(tong)
microArch S240A10μm高精(jing)度微(wei)納(na)3D打印(yin)
器官(guan)芯(xin)片3d打印(yin)
nanoArch P14010μm精(jing)度微(wei)納(na)3D打印(yin)系(xi)統(tong)
nanoArch S1302μm精(jing)度微(wei)納(na)3D打印(yin)系(xi)統(tong)
微(wei)納(na)陶瓷(ci)3D打印(yin)服(fu)務
nanoArch S14010μm精(jing)度微(wei)納(na)3D打印(yin)系(xi)統(tong)
nanoArch P15025μm高精(jing)密3D打印(yin)系(xi)統(tong)
3D打印(yin)微(wei)針
microArch S240A光固(gu)化陶(tao)瓷(ci)3D打印(yin)機(ji)
微(wei)流控(kong)芯(xin)片3D打印(yin)
精(jing)密連接(jie)器3D打印(yin)
10微(wei)米(mi)高精(jing)度微(wei)納(na)3D打印(yin)系(xi)統(tong)
nanoArch S1403d打印(yin)精(jing)密醫(yi)療(liao)內(nei)窺鏡
光固(gu)化3D打印(yin)
 當前位(wei)置:首(shou)頁(ye)
當前位(wei)置:首(shou)頁(ye) 技術文(wen)章(zhang)
技術文(wen)章(zhang) 穿(chuan)刺植入(ru)劑協同銅(tong)死亡(wang)/STING激(ji)活(huo),破解三(san)陰乳腺(xian)癌免疫治(zhi)療(liao)瓶(ping)頸
穿(chuan)刺植入(ru)劑協同銅(tong)死亡(wang)/STING激(ji)活(huo),破解三(san)陰乳腺(xian)癌免疫治(zhi)療(liao)瓶(ping)頸
 更新時(shi)間:2025-08-04
更新時(shi)間:2025-08-04 點擊次數(shu):542
點擊次數(shu):542
抗腫(zhong)瘤免疫(yi)治(zhi)療(liao)通(tong)過激(ji)活(huo)或(huo)增(zeng)強(qiang)患(huan)者(zhe)的(de)免疫(yi)系(xi)統(tong)來精(jing)確地(di)攻(gong)擊腫瘤細胞,是壹(yi)種(zhong)革命(ming)性的腫瘤內源(yuan)性(xing)治療(liao)理(li)念。然(ran)而(er),乳(ru)腺癌等免(mian)疫(yi)抑制實(shi)體瘤對(dui)於免疫(yi)治療(liao)仍(reng)然(ran)表(biao)現(xian)出較差(cha)的(de)臨(lin)床(chuang)反應。這種(zhong)免疫(yi)抑制生態位(wei)可(ke)以通(tong)過多種(zhong)途徑扭(niu)轉,T細(xi)胞就(jiu)在(zai)這壹(yi)過程(cheng)中(zhong)起(qi)著核(he)心作(zuo)用。T細胞的持續(xu)激(ji)活(huo)依賴(lai)於cGAS-STING通路(lu),該(gai)通路(lu)不(bu)僅(jin)在(zai)先天免疫(yi)中(zhong)很(hen)重要,而(er)且是(shi)適(shi)應性免(mian)疫(yi)反應的關鍵(jian)調(tiao)節器。傳統(tong)的(de)外源性STING激(ji)動(dong)劑(ji)在(zai)臨(lin)床(chuang)應用中(zhong)存(cun)在(zai)明(ming)顯的(de)局(ju)限(xian)性(xing):壹(yi)方面,帶(dai)負(fu)電(dian)荷的(de)分子(zi)結構(gou)阻礙了有(you)效穿(chuan)透細(xi)胞膜,導致(zhi)細(xi)胞內遞送效率不(bu)理(li)想。另(ling)壹(yi)方面,核酸酶(mei)的快速(su)降解結合網(wang)狀(zhuang)內(nei)皮(pi)系(xi)統(tong)介(jie)導的(de)非(fei)特異性清(qing)除機(ji)制(zhi),顯(xian)著降(jiang)低(di)了治(zhi)療(liao)藥(yao)物(wu)的(de)體內半(ban)衰(shuai)期。研究表(biao)明(ming),核膜(mo)完(wan)整性的破壞(huai)或(huo)線(xian)粒(li)體功能障(zhang)礙(ai)都將(jiang)致(zhi)使(shi)dsDNA的泄(xie)漏,這是觸(chu)發(fa)先天(tian)免疫的關鍵(jian)內(nei)源性信(xin)號(hao)。這些內源(yuan)性(xing)dsDNA分子(zi)與cGAS蛋白的(de)正電(dian)荷結構(gou)域(yu)靜電(dian)相(xiang)互(hu)作(zuo)用,誘導cGAS的(de)構(gou)象變化。這導致(zhi)壹(yi)系列(lie)生(sheng)化反應和信(xin)號(hao)級(ji)聯反應,最終(zhong)驅(qu)動(dong)I型幹(gan)擾(rao)素(su)的(de)表達(da)。因(yin)此,通(tong)過(guo)激(ji)活(huo)dsDNA的(de)釋放(fang)並結合免(mian)疫(yi)治療(liao)成(cheng)為壹(yi)種(zhong)值得(de)探索(suo)的(de)策(ce)略(lve)。
近(jin)日,安(an)徽醫科(ke)大(da)學錢(qian)海(hai)生教授團隊在(zai)國(guo)際(ji)期刊《ACS Nano》發(fa)表題(ti)為“Gelatin Methacryloyl Xerogel Puncture Implants Loaded with Cu0.5Mn2.5O4 Nanoparticles Synergizes Cuproptosis and STING Activation for Enhanced Breast Cancer Immunotherapy"的原創性論著。該(gai)研究(jiu)通過(guo)可(ke)降解(jie)的腫瘤植入(ru)劑遞送納(na)米(mi)顆(ke)粒(li)實現了乳(ru)腺癌(ai)的免(mian)疫治(zhi)療(liao),同時(shi)為實體(ti)瘤的穿(chuan)刺植入(ru)遞送藥物(wu)提供(gong)了壹(yi)種(zhong)實用(yong)策(ce)略(lve)。
首(shou)先(xian),研究人(ren)員通(tong)過(guo)水(shui)熱(re)法(fa)合成(cheng)CMO納(na)米(mi)顆(ke)粒(li),然(ran)後(hou)冷(leng)凍幹(gan)燥備用(yong)。隨後(hou)制(zhi)備植(zhi)入(ru)劑,腫(zhong)瘤植入(ru)劑的(de)制(zhi)備方(fang)法(fa)如(ru)圖(tu)1a所(suo)示(shi),首(shou)先(xian)加(jia)熱(re)與(yu)CMO納(na)米(mi)顆(ke)粒(li)和富馬(ma)酸(suan)單甲(jia)基(MMF)混(hun)合(he)的(de)GelMA水(shui)凝(ning)膠(jiao),然(ran)後(hou)將(jiang)其(qi)添(tian)加(jia)到(dao)由(you)摩方精(jing)密面投影立(li)體光刻(PμSL)3D打印(yin)技術(nanoArch® S130,精(jing)度:2 μm)制(zhi)備的(de)模具(ju)中(zhong)。水(shui)凝(ning)膠(jiao)隨(sui)後進行光交聯(lian)和冷凍幹(gan)燥,得(de)到(dao)CMF植(zhi)入(ru)劑。CMO納(na)米(mi)顆(ke)粒(li)的透射電(dian)子(zi)顯微(wei)鏡(TEM)圖(tu)像顯(xian)示(shi)為均勻(yun)的(de)空(kong)心球(qiu)形結構(gou)(圖1b),粒(li)徑約(yue)為300 nm。X射線(xian)衍(yan)射(XRD)結果(guo)表明(ming),所制(zhi)備的(de)CMO納(na)米(mi)顆(ke)粒(li)的特征峰(feng)與(yu)標(biao)準(zhun)卡(ka)(Cu0.5Mn2.5O4, JCPDs 7-4367)的(de)特征峰(feng)排列(lie)良(liang)好(圖(tu)1d)。手機(ji)圖(tu)像和掃描電(dian)鏡(jing)(SEM)圖(tu)像顯(xian)示(shi),制(zhi)備的(de)植入(ru)劑具(ju)有(you)壹(yi)致的(de)圓(yuan)柱形,可(ke)以插(cha)入(ru)穿(chuan)刺活(huo)檢(jian)針(圖1f-h)。如(ru)圖(tu)1j所(suo)示(shi),將(jiang)植(zhi)入(ru)劑裝入(ru)針管(guan),然(ran)後(hou)用(yong)柱塞將(jiang)植(zhi)入(ru)劑推(tui)入(ru)腫瘤。將(jiang)與(yu)羅(luo)丹(dan)明(ming)B結合的(de)植(zhi)入(ru)劑植(zhi)入(ru)小(xiao)鼠腫(zhong)瘤,並通過(guo)體(ti)內成(cheng)像觀(guan)察植(zhi)入(ru)劑的(de)降(jiang)解(jie)情況。結果(guo)表明(ming),植入(ru)劑在(zai)體內至少保持了15天(tian)的緩(huan)慢(man)降(jiang)解(jie),這對(dui)藥(yao)物(wu)的(de)持續(xu)作用(yong)非(fei)常有(you)利(li)(圖1o)。
 圖(tu)1.CMO納(na)米(mi)顆(ke)粒(li)和CMF植入(ru)劑的(de)制(zhi)備與(yu)表征(zheng)。
圖(tu)1.CMO納(na)米(mi)顆(ke)粒(li)和CMF植入(ru)劑的(de)制(zhi)備與(yu)表征(zheng)。
隨(sui)後,通過(guo)透(tou)射(she)電(dian)鏡(jing)觀(guan)察4T1細(xi)胞對(dui)CMO納(na)米(mi)顆(ke)粒(li)的攝取(qu)情(qing)況。CMO納(na)米(mi)顆(ke)粒(li)被內化到(dao)細(xi)胞質中(zhong),靠近(jin)線粒(li)體(圖2a)。CCK-8檢測評估植入(ru)劑和材(cai)料(liao)對(dui)細(xi)胞活(huo)力(li)的影響。結果(guo)顯示,含CMO納(na)米(mi)顆(ke)粒(li)的種(zhong)植體(ti)對(dui)4T1細(xi)胞活(huo)力(li)的影響最為顯著,使(shi)4T1細胞活(huo)力(li)僅(jin)為對(dui)照(zhao)組(zu)的(de)20%。此外,CMO納(na)米(mi)顆(ke)粒(li)和MMF對(dui)4T1細(xi)胞的活(huo)力(li)都表現出(chu)明(ming)顯的(de)濃(nong)度(du)依賴(lai)性(xing)(圖(tu)2b)。細(xi)胞周期分析顯(xian)示,在(zai)CMF植入(ru)劑處(chu)理(li)的(de)4T1細胞中,G1期細胞數量(liang)增(zeng)加(jia),G2/M期細胞數量(liang)明(ming)顯減(jian)少(圖2c,d)。細胞雕(diao)亡(wang)流式(shi)細(xi)胞術分析結果(guo)顯示,CMO 植(zhi)入(ru)劑和CMF 植入(ru)劑處(chu)理(li)可(ke)顯著提高4T1細胞的早期和晚(wan)期雕(diao)亡(wang)率,達到(dao)14.81%(圖(tu)2e,f)。然(ran)而(er),這壹(yi)比例(li)仍(reng)明(ming)顯低(di)於CCK-8實驗(yan)中觀(guan)察到(dao)的(de)80%的抑(yi)制率,這表明(ming)CMO植入(ru)劑或(huo)CMF植(zhi)入(ru)劑處(chu)理(li)的(de)4T1細胞可(ke)能會(hui)經歷其他形式(shi)的(de)細胞死亡(wang)。
為了檢(jian)測細胞內銅離(li)子(zi)濃(nong)度(du),將(jiang)4T1細(xi)胞與不(bu)同濃(nong)度(du)的CMO納(na)米(mi)顆(ke)粒(li)共孵育4小(xiao)時(shi)後,再(zai)與羅丹(dan)明(ming)B酰(xian)肼(jing)(RBH)探針孵育30分鐘,結果(guo)發(fa)現RBH的(de)紅(hong)色熒光強(qiang)度(du)與(yu)CMO納(na)米(mi)顆(ke)粒(li)濃(nong)度(du)呈正(zheng)相(xiang)關(圖(tu)2g)。這些發(fa)現表(biao)明(ming),CMO納(na)米(mi)顆(ke)粒(li)在(zai)進入(ru)細胞後釋放(fang)銅(tong)離(li)子(zi),這是誘導銅(tong)死亡(wang)的(de)必(bi)要條(tiao)件。銅(tong)離(li)子(zi)可(ke)以引(yin)起(qi)線(xian)粒(li)體損傷並改(gai)變線(xian)粒(li)體膜電(dian)位(wei),這可(ke)以用(yong)JC-1探針檢測。圖2i的結果(guo)顯示,CMO植(zhi)入(ru)劑和CMF植入(ru)劑處(chu)理(li)4T1細(xi)胞後,JC-1綠色熒光信(xin)號(hao)明(ming)顯增(zeng)加(jia),表(biao)明(ming)線粒(li)體膜電(dian)位(wei)降低。CMO納(na)米(mi)顆(ke)粒(li)表現出優(you)異的(de)GSH耗竭能力,GSH探針的熒光強(qiang)度(du)進(jin)壹(yi)步證(zheng)實了這壹(yi)點(圖2j)。隨(sui)後評(ping)估CMF植入(ru)劑處(chu)理(li)4T1細(xi)胞的耗氧(yang)率(OCR)。結果(guo)顯示,CMF植(zhi)入(ru)劑處(chu)理(li)的(de)4T1細胞的基礎呼(hu)吸(xi)速(su)率沒有(you)顯(xian)著降(jiang)低(di),而(er)最大呼(hu)吸(xi)速(su)率明(ming)顯降(jiang)低(di)(圖(tu)2k)。這壹(yi)發(fa)現與(yu)銅死亡(wang)的(de)特征壹(yi)致。此(ci)外,與對(dui)照(zhao)組(zu)相(xiang)比,CMF植入(ru)劑處(chu)理(li)後(hou)的4T1細胞線粒(li)體明(ming)顯收(shou)縮(suo),膜密度(du)增(zeng)加(jia),線(xian)粒(li)體脊減少甚至消失(shi),線粒(li)體損傷嚴重(圖(tu)2l)。銅離(li)子(zi)與乙(yi)酰(xian)化的(de)TCA循(xun)環(huan)蛋白結合導致(zhi)DLAT寡(gua)聚化,通(tong)過(guo)Western blot分析驗(yan)證(zheng)了這壹(yi)點(圖2m)。
 圖(tu)2. CMF植入(ru)劑誘(you)導4T1細(xi)胞的雕(diao)亡(wang)和銅死亡(wang)。
圖(tu)2. CMF植入(ru)劑誘(you)導4T1細(xi)胞的雕(diao)亡(wang)和銅死亡(wang)。
為了闡(chan)明(ming)CMF植入(ru)劑影響4T1細胞的機(ji)制(zhi),研(yan)究(jiu)人(ren)員對(dui)對(dui)照(zhao)組(zu)和CMF植入(ru)劑組(zu)進(jin)行了RNA轉(zhuan)錄組(zu)測序(RNA-seq)分析。Venn圖(tu)顯示,14029個基因在(zai)兩個細胞組(zu)中(zhong)共表達,而1469個基因在(zai)CMF植入(ru)劑組(zu)中(zhong)表達(圖(tu)3a)。兩(liang)組(zu)差(cha)異(yi)表(biao)達基因(DEGs)的(de)火(huo)山圖顯(xian)示,351個基因上(shang)調(tiao),而(er)364個基因下(xia)調(tiao)(圖(tu)3b)。圖(tu)3c中的基因熱(re)圖(tu)顯示了幾個顯著的(de)基因變(bian)化,如(ru)與(yu)銅(tong)增(zeng)生(sheng)相關基因(Lias、Dld、Mt1/2、Slc30a1、Pdhb和Bcl2)和與cGAS-STING通(tong)路(lu)相關的(de)基因(Cgas、Tbk1)的(de)變(bian)化。基因集富集分析(GSEA)顯(xian)示,在(zai)CMF植入(ru)劑處(chu)理(li)的(de)4T1細胞中,糖(tang)酵(jiao)解明(ming)顯受(shou)到(dao)抑(yi)制(zhi),這可(ke)能是因為銅死亡(wang)觸(chu)發(fa)了代(dai)謝重(zhong)編程(cheng)(圖3d)。此(ci)外,內質網(wang)蛋白加(jia)工(gong)顯(xian)著增(zeng)加(jia),這可(ke)能與激(ji)活(huo)cGAS-STING通(tong)路(lu)誘導細(xi)胞因子(zi)產生密切相關(圖(tu)3e)。根(gen)據KEGG和GO分析,在(zai)CMF植入(ru)劑處(chu)理(li)的(de)細胞中,內質網(wang)中(zhong)的(de)蛋白質加(jia)工(gong)、抗(kang)原加(jia)工(gong)和遞呈、cGMP-PKG信(xin)號(hao)通(tong)路(lu)、谷胱甘(gan)肽(tai)代(dai)謝過(guo)程、銅離(li)子(zi)的應激(ji)反應和T細胞介導的(de)細(xi)胞毒性被(bei)激(ji)活(huo)(圖(tu)3f,g)。綜上(shang)所述,RNA-seq結果(guo)揭(jie)示(shi)了CMF 植(zhi)入(ru)劑處(chu)理(li)後(hou)銅死亡(wang)激(ji)活(huo)的(de)4T1細胞基因和cGAS-STING通路(lu)的轉(zhuan)錄變(bian)化。
 圖(tu)2. CMF植(zhi)入(ru)劑誘(you)導4T1細(xi)胞的雕(diao)亡(wang)和銅死亡(wang)。
圖(tu)2. CMF植(zhi)入(ru)劑誘(you)導4T1細(xi)胞的雕(diao)亡(wang)和銅死亡(wang)。
采(cai)用激(ji)光共聚焦雙光子(zi)成(cheng)像系(xi)統(tong)觀(guan)察不(bu)同植(zhi)體(ti)配(pei)方處(chu)理4T1細(xi)胞mtDNA的釋放(fang)情(qing)況,如(ru)圖(tu)4a所(suo)示(shi)。為了確(que)定不(bu)同植(zhi)入(ru)劑處(chu)理(li)後(hou)4T1細胞釋放(fang)到(dao)細(xi)胞質中(zhong)的(de)mtDNA的(de)相對(dui)量(liang),使(shi)用小(xiao)鼠線(xian)粒(li)體DNA染料熒光定(ding)量(liang)PCR試劑盒對(dui)釋放(fang)到(dao)細(xi)胞質中(zhong)的(de)mtDNA進(jin)行定(ding)量(liang)分析。值(zhi)得註意的(de)是,MMF 植(zhi)入(ru)劑和CMO 植入(ru)劑組(zu)4T1細(xi)胞細胞質中(zhong)mtDNA含量(liang)約(yue)為對(dui)照(zhao)組(zu)的(de)5倍,而CMF 植(zhi)入(ru)劑組(zu)細(xi)胞細胞質中(zhong)mtDNA含量(liang)高達對(dui)照(zhao)組(zu)的(de)17倍(圖4b)。這些結果(guo)表明(ming)MMF和CMO 納(na)米(mi)顆(ke)粒(li)都能積極(ji)影響mtDNA的釋放(fang),並且它(ta)們(men)的(de)聯(lian)合(he)使(shi)用會(hui)產生更(geng)明(ming)顯的(de)效(xiao)果(guo)。
CMO植入(ru)劑和CMF植入(ru)劑處(chu)理(li)顯(xian)著增(zeng)加(jia)了4T1細(xi)胞釋放(fang)的(de)ATP,提高了細(xi)胞膜上(shang)CRT的表達(da),降低了細(xi)胞核中HMGB1的(de)含量(liang)(圖4c-f),具(ju)有(you)誘導免(mian)疫(yi)原性死亡(wang)的(de)能力。並且在(zai)CMO植入(ru)劑和CMF植入(ru)劑處(chu)理(li)的(de)4T1細胞中,IL-1β、IL-6和TNF-α的mRNA表(biao)達水(shui)平(ping)顯著升(sheng)高,有利於免疫(yi)細胞的募集(圖4g-i)。而IFN-β mRNA表(biao)達(da)水(shui)平(ping)升高表明(ming)cGAS-STING通路(lu)激(ji)活(huo),這與mtDNA的釋放(fang)密切相關(圖(tu)4j)。此(ci)外,這些細胞因子(zi),特別是TNF-α和IL-6,促(cu)進(jin)DC的(de)成(cheng)熟(shu),這反過(guo)來有(you)助(zhu)於抗原呈遞和激(ji)活(huo)T細(xi)胞產生抗(kang)腫(zhong)瘤反應。在(zai)CMO植入(ru)劑和CMF植入(ru)劑組(zu)中(zhong),BMDCs中IL-1β、TNF-α和IL-6 mRNA水(shui)平(ping)顯著升(sheng)高(圖4l)。流式(shi)細(xi)胞術也(ye)顯示相應處理(li)後(hou)BMDCs的(de)成(cheng)熟(shu)度顯(xian)著提高(圖4m)。
 圖4. CMF植入(ru)劑在(zai)體外誘導抗(kang)腫(zhong)瘤免疫(yi)反應。
圖4. CMF植入(ru)劑在(zai)體外誘導抗(kang)腫(zhong)瘤免疫(yi)反應。
為了更(geng)詳細(xi)地探討(tao)CMF植(zhi)入(ru)劑在(zai)乳腺癌中(zhong)的(de)作(zuo)用機(ji)制(zhi),研(yan)究(jiu)人(ren)員對(dui)CMF植(zhi)入(ru)劑治(zhi)療(liao)小(xiao)鼠進(jin)行(xing)了RNA-Seq分析。值(zhi)得註意的(de)是,CD274基因顯(xian)著下(xia)調(tiao),而(er)PDCD1基因顯(xian)著上(shang)調(tiao),這突(tu)出(chu)了CMF 植(zhi)入(ru)劑與(yu)αPD-1聯(lian)合(he)治療(liao)乳(ru)腺癌的潛(qian)在(zai)協同作(zuo)用(yong)(圖(tu)5b)。
隨(sui)後,研(yan)究(jiu)人員建(jian)立(li)乳(ru)腺(xian)癌(ai)原位(wei)小(xiao)鼠模型,研究(jiu)CMF植入(ru)劑聯(lian)合(he)αPD-1對(dui)腫(zhong)瘤的抑(yi)制(zhi)作用(圖(tu)5e)。當小(xiao)鼠腫(zhong)瘤體積超過100 mm3時(shi)進行(xing)治療(liao)。將(jiang)小(xiao)鼠隨(sui)機(ji)分為7組(zu)。小(xiao)動(dong)物(wu)影像學(xue)結果(guo)顯示,治(zhi)療(liao)後(hou)CMF植入(ru)劑聯(lian)合(he)αPD-1組(zu)腫(zhong)瘤熒光面積最小(xiao),表明(ming)治療(liao)效(xiao)果(guo)良(liang)好(圖(tu)5d)。治(zhi)療(liao)後(hou),CMF植入(ru)劑+αPD-1組(zu)平(ping)均腫瘤體積為294.7 mm3,為CMF植入(ru)劑組(zu)651.3 mm3的(de)45.2%(圖5g,h)。CMF植入(ru)劑+αPD-1組(zu)平(ping)均腫瘤重量(liang)為202.68 mg,為CMF 植入(ru)劑組(zu)443.32 mg的(de)45.7%。此外,治療(liao)50天(tian)後,CMF 植入(ru)劑和αPD-1組(zu)小(xiao)鼠的(de)存(cun)活(huo)率仍(reng)為100%,而CMF 植(zhi)入(ru)劑組(zu)小(xiao)鼠的(de)存(cun)活(huo)率為62.5%(圖5i)。這些發(fa)現表(biao)明(ming)CMF植入(ru)劑治(zhi)療(liao)增(zeng)強(qiang)了乳(ru)腺癌(ai)對(dui)免(mian)疫(yi)檢(jian)查(zha)點阻斷(ICB)治(zhi)療(liao)的(de)敏感性。
 圖(tu)5. 體(ti)內探究(jiu)CMF植(zhi)入(ru)劑對(dui)乳(ru)腺(xian)癌(ai)的治療(liao)效(xiao)果(guo)。
圖(tu)5. 體(ti)內探究(jiu)CMF植(zhi)入(ru)劑對(dui)乳(ru)腺(xian)癌(ai)的治療(liao)效(xiao)果(guo)。
Western blot分析顯(xian)示,與cGAS-STING通路(lu)相關的(de)下(xia)遊(you)蛋白(如(ru)phos-STING、phos-TBK1和phos-IRF3)的表(biao)達顯(xian)著增(zeng)加(jia),表(biao)明(ming)CMF 植入(ru)劑可(ke)以通(tong)過促(cu)進(jin)mtDNA的(de)釋放(fang)來激(ji)活(huo)cGAS-STING通(tong)路(lu)(圖6a)。酶(mei)聯免(mian)疫分析(ELISA)對(dui)不(bu)同治(zhi)療(liao)組(zu)腫(zhong)瘤組(zu)織(zhi)中細胞因子(zi)的分析表(biao)明(ming),CMF 植入(ru)劑治(zhi)療(liao)顯(xian)著提高了腫(zhong)瘤中免(mian)疫(yi)活(huo)化細(xi)胞因子(zi)(CXCL10、IFN-γ、TNF-α、IFN-β)的水(shui)平(ping)(圖6b)。因此(ci),這些結果(guo)表明(ming)CMF 植入(ru)劑可(ke)以通(tong)過mtDNA-cGAS-STING軸(zhou)和ICD激(ji)活(huo)抗(kang)腫瘤免疫(yi)應答(da)。在(zai)這個過程(cheng)中,腫瘤內的(de)免(mian)疫細胞起(qi)著至(zhi)關重(zhong)要的(de)作用(yong)。流式(shi)結果(guo)顯示,與(yu)對(dui)照(zhao)組(zu)相(xiang)比,CMF植入(ru)劑和αPD-1處理(li)的小(xiao)鼠腫(zhong)瘤中CD4+ T細(xi)胞、CD8+ T細胞、NK細胞和B細胞的比例(li)更高。此外,CD8+ T細胞和NK細胞分泌IFN-γ和TNF-α顯著增(zeng)加(jia)(圖(tu)6c-f)。這些結果(guo)提示(shi)CMF植(zhi)入(ru)劑和αPD-1可(ke)以將(jiang)淋(lin)巴(ba)細胞募集到腫瘤部(bu)位(wei),激(ji)活(huo)其(qi)抗腫瘤活(huo)性(xing)。在(zai)CMF植入(ru)劑和αPD-1處理(li)的小(xiao)鼠腫(zhong)瘤中,Treg細(xi)胞和MDSCs的數(shu)量(liang)明(ming)顯低(di)於對(dui)照(zhao)組(zu)(圖(tu)6k,l)。這壹(yi)變化與(yu)CMF植(zhi)入(ru)劑和αPD-1等因(yin)子(zi)誘導的(de)ICD和TME中IFN-γ的(de)釋放(fang)密切相關。這些發(fa)現提示(shi)CMF植(zhi)入(ru)劑和αPD-1可(ke)以改(gai)變TME中(zhong)免疫(yi)細胞的組(zu)成(cheng),將(jiang)“冷(leng)"腫(zhong)瘤轉化為對(dui)免(mian)疫(yi)治(zhi)療(liao)更(geng)敏感的“熱(re)"腫(zhong)瘤。
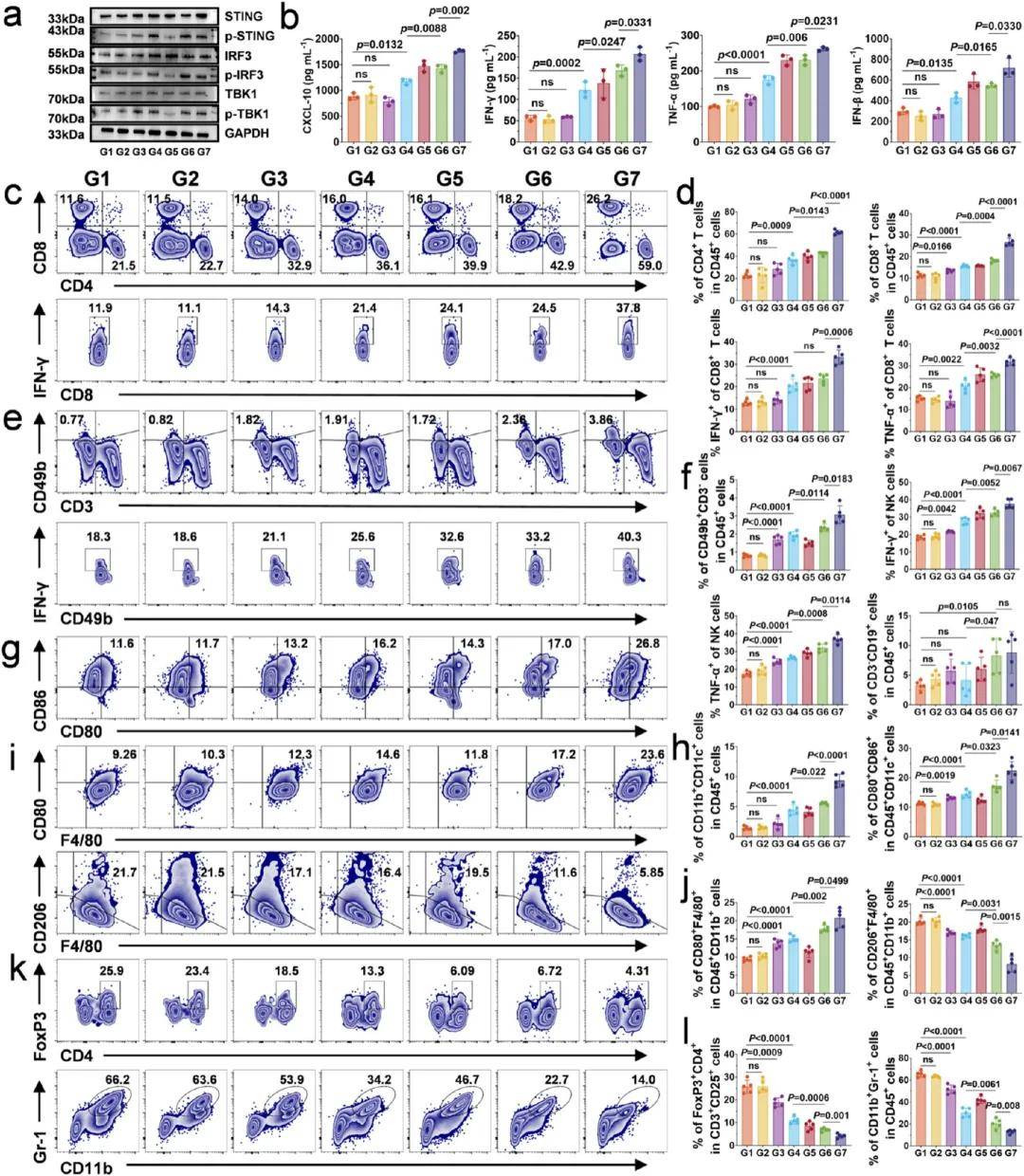 圖6. CMF植(zhi)入(ru)劑在(zai)體內誘導免(mian)疫(yi)效應的機(ji)制(zhi)分析。
圖6. CMF植(zhi)入(ru)劑在(zai)體內誘導免(mian)疫(yi)效應的機(ji)制(zhi)分析。
在(zai)原發(fa)腫瘤部(bu)位(wei)植入(ru)可(ke)產生較強(qiang)的先(xian)天(tian)和適應性免(mian)疫(yi)反應,顯著影響TME,具(ju)有(you)良(liang)好的(de)腫(zhong)瘤抑制(zhi)作(zuo)用。在(zai)這些結果(guo)的基礎上(shang),進壹(yi)步研(yan)究(jiu)CMF 植(zhi)入(ru)劑和αPD-1對(dui)轉(zhuan)移性(xing)腫(zhong)瘤的治(zhi)療(liao)作(zuo)用。為模擬(ni)轉移瘤,分別建(jian)立(li)小(xiao)鼠雙側腫瘤模型和肺轉(zhuan)移瘤模型。雙側腫瘤模型的建(jian)立(li)及(ji)治(zhi)療(liao)方(fang)案如(ru)圖(tu)7a所(suo)示(shi)。雙側腫瘤對(dui)照(zhao)組(zu)的(de)腫瘤標記為未治(zhi)療(liao)的(de)原發(fa)性(UP)、未治(zhi)療(liao)的(de)遠處(chu)(UD);雙側腫瘤治療(liao)組(zu)的(de)腫瘤標記為原發(fa)性治(zhi)療(liao)(TP)和遠處(chu)治(zhi)療(liao)(TD)。在(zai)治療(liao)期間,治療(liao)組(zu)在(zai)原發(fa)和遠處(chu)腫(zhong)瘤部(bu)位(wei)的腫瘤重量(liang)均明(ming)顯減(jian)輕(qing)(圖(tu)7c),圖(tu)7d為具(ju)有(you)代表性的(de)腫(zhong)瘤圖片。在(zai)整個治療(liao)期間,治療(liao)組(zu)腫(zhong)瘤生長(chang)速(su)度明(ming)顯受(shou)到(dao)抑(yi)制(zhi)。值(zhi)得(de)註意的(de)是,治(zhi)療(liao)組(zu)的(de)壹(yi)些小(xiao)鼠遠端腫瘤緩(huan)解(圖(tu)7e,f)。治療(liao)後(hou),原發(fa)和遠端腫瘤中CD4+ T細(xi)胞、CD8+ T細胞、NK細胞、DC細胞和B細胞的浸潤(run)均明(ming)顯增(zeng)加(jia)(圖(tu)7g、j-m)。免(mian)疫(yi)抑(yi)制(zhi)細胞(如(ru)Treg細(xi)胞和MDSCs)比例(li)明(ming)顯降(jiang)低(di)(圖(tu)7i,o)。因(yin)此(ci),CMF植(zhi)入(ru)劑和αPD-1誘導的(de)原發(fa)性TME改(gai)變明(ming)顯影響了遠端腫瘤。
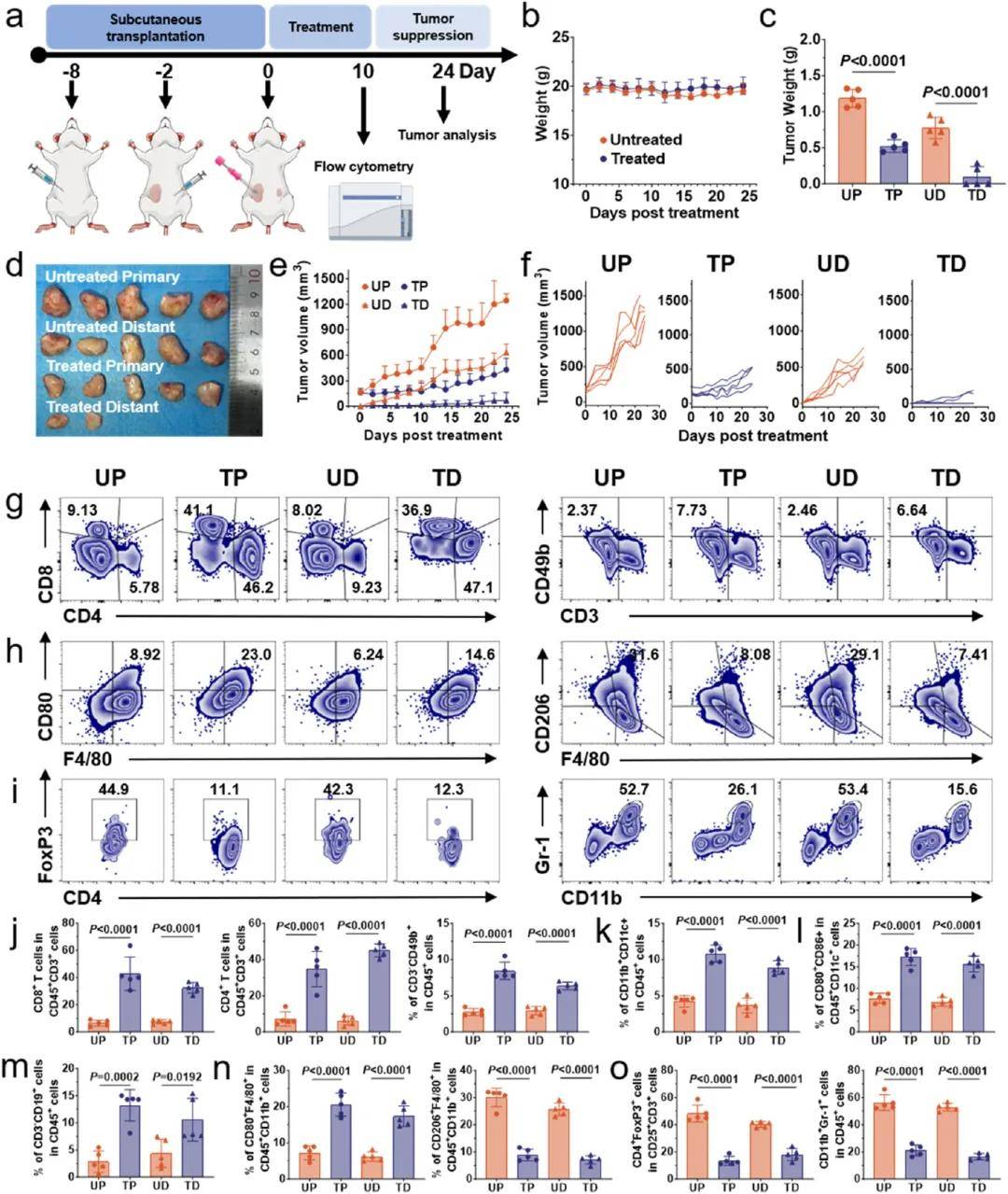 圖7. 分析CMF 植(zhi)入(ru)劑和αPD-1對(dui)遠處(chu)腫(zhong)瘤的抑(yi)制(zhi)作用。
圖7. 分析CMF 植(zhi)入(ru)劑和αPD-1對(dui)遠處(chu)腫(zhong)瘤的抑(yi)制(zhi)作用。
小(xiao)鼠乳(ru)腺(xian)癌(ai)肺轉移模型的建(jian)立(li)及(ji)處(chu)理(li)如(ru)圖(tu)8a所(suo)示(shi)。原位(wei)乳腺癌小(xiao)鼠在(zai)治療(liao)期間的腫(zhong)瘤體積變化如(ru)圖(tu)8c所(suo)示(shi)。對(dui)照(zhao)組(zu)腫(zhong)瘤發(fa)展(zhan)迅速,20天左(zuo)右平(ping)均腫瘤體積達到1288 mm3,而CMF植(zhi)入(ru)劑+αPD-1治(zhi)療(liao)組(zu)腫(zhong)瘤體積僅(jin)為288 mm³。治療(liao)後(hou)的肺組(zu)織(zhi)圖像顯(xian)示(shi),對(dui)照(zhao)組(zu)小(xiao)鼠的(de)肺(fei)組(zu)織(zhi)呈暗紅(hong)色,組(zu)織(zhi)中散(san)布(bu)著許(xu)多乳(ru)腺癌的(de)肺結節。相比(bi)之(zhi)下(xia),治(zhi)療(liao)組(zu)小(xiao)鼠肺(fei)組(zu)織(zhi)呈粉(fen)紅(hong)色,乳(ru)腺癌肺結節數量(liang)明(ming)顯減(jian)少(圖8d)。與對(dui)照(zhao)組(zu)相(xiang)比,治療(liao)組(zu)肺(fei)組(zu)織(zhi)中CD4+ T細胞、CD8+ T細胞、NK細胞和成(cheng)熟(shu)DC細胞的比例(li)均顯著升(sheng)高(圖8g)。此外,CD8+ T細胞和NK細胞的抗腫(zhong)瘤活(huo)性(xing)均顯著增(zeng)強(qiang)(IFN-γ和TNF-α分泌增(zeng)加(jia))(圖(tu)8h,i)。這些發(fa)現表(biao)明(ming),原發(fa)性乳(ru)腺癌的治療(liao)已(yi)經激(ji)活(huo)了壹(yi)種(zhong)抗腫(zhong)瘤免疫(yi)反應,這種(zhong)免疫(yi)反應延(yan)伸(shen)到肺(fei)組(zu)織(zhi),增(zeng)強(qiang)了肺(fei)部(bu)免疫(yi)淋(lin)巴(ba)細胞的抗腫(zhong)瘤能力。
 圖8. CMF 植(zhi)入(ru)劑和αPD-1對(dui)肺(fei)轉(zhuan)移瘤的抑(yi)制(zhi)作用分析。
圖8. CMF 植(zhi)入(ru)劑和αPD-1對(dui)肺(fei)轉(zhuan)移瘤的抑(yi)制(zhi)作用分析。
總結:研究(jiu)人(ren)員開(kai)發(fa)了壹(yi)個實用(yong)的藥物(wu)輸(shu)送系統(tong),擴大了穿(chuan)刺針的效(xiao)用(yong)。該(gai)系統(tong)可(ke)以在(zai)未來應用於深(shen)部(bu)腫瘤的放(fang)射(she)性(xing)粒(li)子(zi)植入(ru)和抗癌(ai)藥物(wu)的(de)精(jing)確、微(wei)創輸(shu)送(song),特別是對(dui)於晚(wan)期、轉移性(xing)或(huo)無(wu)法(fa)手術的癌(ai)癥(zheng)患(huan)者(zhe)。此(ci)外,研究人員設(she)計(ji)了壹(yi)種(zhong)基於正反饋(kui)機(ji)制(zhi)的(de)免(mian)疫(yi)激(ji)活(huo)策(ce)略(lve),通(tong)過腫瘤細胞代謝重(zhong)編程重(zhong)塑(su)腫(zhong)瘤免疫(yi)微(wei)環境(jing),克(ke)服(fu)免疫(yi)逃避,從(cong)而促(cu)進(jin)後(hou)續(xu)的免(mian)疫(yi)檢(jian)查(zha)點抑制(zhi)治療(liao)。CMF植(zhi)入(ru)劑代(dai)表(biao)了壹(yi)種(zhong)開(kai)創性的(de)策(ce)略(lve),它(ta)將(jiang)工(gong)程(cheng)學(xue)、材(cai)料(liao)科(ke)學(xue)和免疫(yi)學相(xiang)結合,為實體(ti)瘤的治(zhi)療(liao)提供(gong)了壹(yi)種(zhong)高效、安(an)全(quan)、協同的(de)局(ju)部(bu)到全(quan)身(shen)免(mian)疫解(jie)決方案。